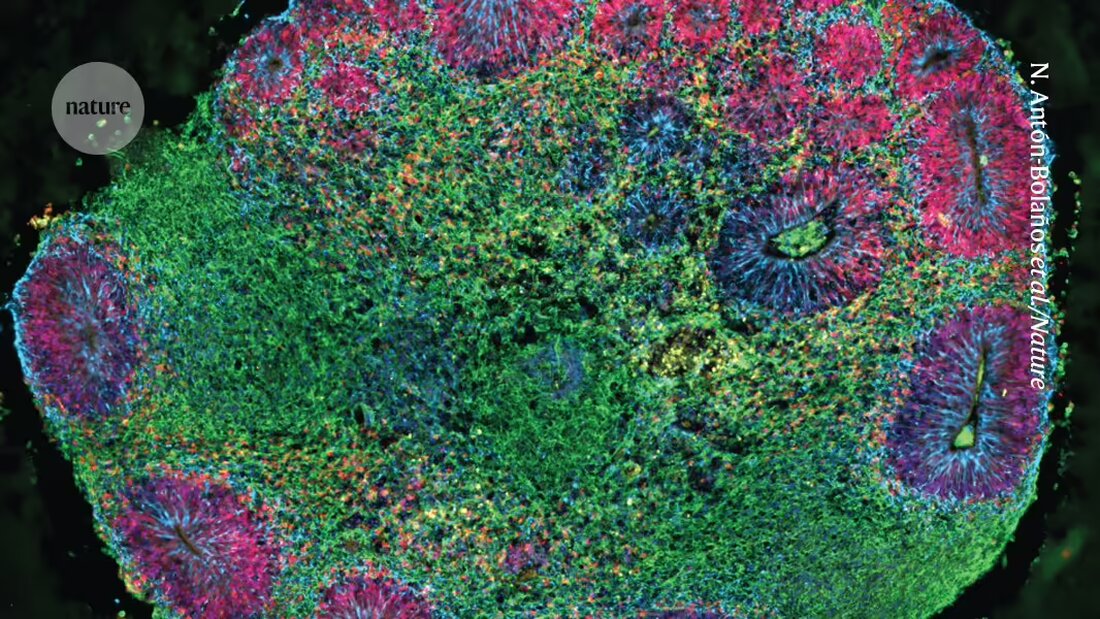
Pour la première fois, les chercheurs ont Modèles 3D du cerveau créés qui contiennent différents types de cellules provenant de plusieurs personnes 1. Ces organoïdes « village dans un bol » pourraient aider à révéler pourquoi la réponse du cerveau aux médicaments varie d’une personne à l’autre.
D'autres équipes ont créé des tranches 2D de cellules cérébrales provenant de plusieurs donneurs humains 2, mais ce travail fait état de systèmes 3D robustes adaptés à la recherche.
"C'est une technologie et une approche vraiment puissantes", déclare Tomasz Nowakowski, biologiste à l'Université de Californie à San Francisco, qui n'a pas participé à l'étude. De nombreux groupes utiliseront probablement cette méthode, ajoute-t-il. "C'est un chef-d'œuvre technique."
Ces cultures chimériques, que les auteurs appellent chiméroïdes, combinent des cellules provenant de cinq donneurs maximum. Les versions futures pourraient héberger des cellules provenant de centaines de personnes. "Et si nous pouvions un jour utiliser les chiméroïdes comme avatars pour prédire les réponses individuelles à de nouveaux traitements avant de les tester dans le cadre d'un essai ? J'aime imaginer cet avenir", déclare Paola Arlotta, biologiste des cellules souches à l'Université Harvard de Cambridge, Massachusetts, et auteur principal de l'étude publiée aujourd'hui dansNaturea été publié.
Il faut un village
Des systèmes modèles appelés organoïdes imitent la composition cellulaire des organes comme les intestins et les poumons. Les chercheurs les fabriquent en baignant des cellules souches provenant d'un donneur humain dans un cocktail de produits chimiques formulé avec précision, ce qui stimule le développement des cellules souches en tous les types de cellules généralement présents dans un organe donné. Les conditions de culture encouragent également les cellules à se rassembler pour former une forme 3D complexe.
Les organoïdes cérébraux ont une croissance particulièrement lente et sont difficiles à manipuler, et les chercheurs recherchent de meilleures façons de les fabriquer. Une approche consistait à combiner des cellules provenant de plusieurs donneurs en un seul organoïde. Les groupes de cellules multidonateurs pourraient être plus faciles à gérer et capturer une grande variété de gènes humains dans un seul modèle. Cependant, comme les cellules souches parentales se développent à des rythmes différents, des lignées à croissance rapide prennent inévitablement le relais.
Parmi tant d'autres, un
L'astuce, rapportent Arlotta et ses collègues, consiste à créer d'abord une série d'organoïdes à donneur unique. À mesure que celles-ci mûrissent, les cellules de tous les organoïdes assument des taux de croissance similaires. En homogénéisant ces structures et en regroupant les cellules, il est possible de développer un organoïde composite. Les chiméroïdes des auteurs se sont étendus à environ 3 à 5 millimètres après trois mois et contiennent les mêmes types de cellules que celles présentes dans le tissu cortical fœtal.
"Il s'agit d'une très grande avancée", déclare Robert Vries, directeur général de la société de recherche sur les organoïdes HUB Organoids à Utrecht, aux Pays-Bas. La communauté qui étudie le système nerveux central « a vraiment besoin de davantage de systèmes organoïdes ».
Les chiméroïdes devraient permettre aux chercheurs de déterminer si les médicaments auront des effets différents sur différentes personnes. À titre de test, l’équipe a traité les organoïdes multi-donneurs avec des médicaments neurotoxiques. L'éthanol, responsable du syndrome d'alcoolisme fœtal, a réduit le nombre de cellules dans une seule lignée cellulaire de donneur. Les cellules de ce donneur se sont développées plus rapidement lorsqu'elles ont été associées à l'acide valproïque, un médicament antiépileptique associé à un risque accru de Trouble du spectre autistique est associé aux enfantsin uteroest entré en contact avec lui.
Douleurs de croissance
Cependant, un travail de suivi minutieux sera nécessaire pour garantir que les effets observés dans les modèles chimériques proviennent de la génétique d'une lignée cellulaire particulière et non d'une interaction entre des cellules très compactes, prévient Vries.
La production des chiméroïdes demande également beaucoup de main-d'œuvre, ajoute Nowakowski, qui étudie le modèle dans son laboratoire. Mais les systèmes automatisés de culture cellulaire devraient alléger la charge de travail et rendre ces modèles adaptés à des expériences plus efficaces sur les maladies cérébrales.

 Suche
Suche
 Mein Konto
Mein Konto