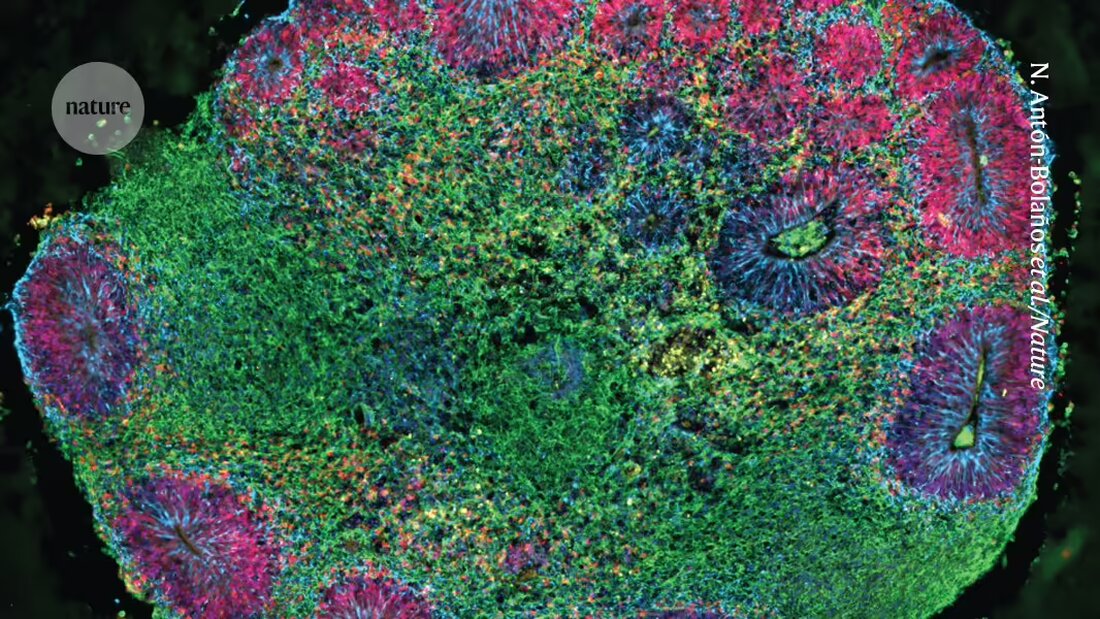
Voor het eerst hebben onderzoekers dat gedaan 3D-modellen van de hersenen gemaakt die verschillende celtypen van meerdere mensen bevatten 1. Deze ‘dorp in een kom’-organoïden kunnen helpen onthullen waarom de reactie van de hersenen op medicijnen van persoon tot persoon verschilt.
Andere teams hebben 2D-plakjes van hersencellen gemaakt van meer dan één menselijke donor 2, maar dit werk rapporteert robuuste 3D-systemen die geschikt zijn voor onderzoek.
“Het is een heel krachtige technologie en aanpak”, zegt Tomasz Nowakowski, een bioloog aan de Universiteit van Californië, San Francisco, die niet bij het onderzoek betrokken was. Veel groepen zullen deze methode waarschijnlijk gebruiken, voegt hij eraan toe. “Het is een technisch meesterwerk.”
Deze chimere culturen, die de auteurs chimeroïden noemen, combineren cellen van maximaal vijf donoren. Toekomstige versies zouden cellen van honderden mensen kunnen huisvesten. "Wat als we op een dag chimeroïden als avatars zouden kunnen gebruiken om individuele reacties op nieuwe therapieën te voorspellen voordat we ze in een proef testen? Ik stel me die toekomst graag voor", zegt Paola Arlotta, een stamcelbioloog aan de Harvard University in Cambridge, Massachusetts, en senior auteur van de studie die vandaag is gepubliceerd inNatuurwerd gepubliceerd.
Er is een dorp voor nodig
Modelsystemen, organoïden genoemd, bootsen de cellulaire samenstelling van organen na zoals darmen en longen. Onderzoekers maken ze door stamcellen van een menselijke donor te baden in een nauwkeurig geformuleerde cocktail van chemicaliën, die de stamcellen stimuleert zich te ontwikkelen tot alle celtypen die doorgaans in een bepaald orgaan aanwezig zijn. De kweekomstandigheden moedigen de cellen ook aan om samen te komen in een complexe 3D-vorm.
Hersenorganoïden groeien bijzonder langzaam en zijn moeilijk te hanteren, en onderzoekers zoeken naar betere manieren om ze te maken. Eén benadering was om cellen van meerdere donoren te combineren tot één organoïde. Multidonorcelclusters zouden gemakkelijker te hanteren kunnen zijn en een grote verscheidenheid aan menselijke genetica in één enkel model kunnen vastleggen. Omdat de ouderstamcellen echter met verschillende snelheden groeien, nemen snelgroeiende lijnen het onvermijdelijk over.
Uit velen één
De truc, zo melden Arlotta en haar collega's, is om eerst een reeks organoïden met één donor te maken. Naarmate deze volwassener worden, nemen de cellen in alle organoïden vergelijkbare groeisnelheden aan. Door deze structuren te homogeniseren en de cellen samen te voegen, is het mogelijk een samengestelde organoïde te laten groeien. De chimeroïden van de auteurs zijn na drie maanden uitgegroeid tot ongeveer 3-5 millimeter en bevatten dezelfde celtypen als aanwezig in foetaal corticaal weefsel.
“Dit is echt een grote vooruitgang”, zegt Robert Vries, directeur van organoïdenonderzoeksbedrijf HUB Organoids in Utrecht, Nederland. De gemeenschap die het centrale zenuwstelsel bestudeert “heeft echt meer organoïdesystemen nodig.”
Chimeroïden moeten onderzoekers in staat stellen erachter te komen of medicijnen verschillende effecten op verschillende mensen zullen hebben. Als testcase behandelde het team de multidonor-organoïden met neurotoxische medicijnen. Ethanol, dat het foetaal alcoholsyndroom veroorzaakt, verminderde het aantal cellen in een enkele donorcellijn. Cellen van deze donor groeiden sneller in combinatie met valproïnezuur, een anti-epilepticum dat in verband wordt gebracht met een verhoogd risico op Autismespectrumstoornis wordt geassocieerd met kinderenin de baarmoederermee in aanraking kwam.
Groeipijnen
Er zal echter zorgvuldig vervolgwerk nodig zijn om ervoor te zorgen dat de effecten die in de chimere modellen worden waargenomen voortkomen uit de genetica van een bepaalde cellijn en niet uit een interactie tussen dicht opeengepakte cellen, waarschuwt Vries.
Chimeroïden zijn ook arbeidsintensief om te produceren, zegt Nowakowski, die het model in zijn laboratorium bestudeert. Maar geautomatiseerde celcultuursystemen zouden de werklast moeten verlichten en deze modellen geschikt moeten maken voor efficiëntere experimenten met hersenziekten.

 Suche
Suche
 Mein Konto
Mein Konto